الصيغة الكيميائية من الغليسرين. الصيغة الهيكلية والجزيئية
أبسط الكحول polyhydric ، الذي فيههناك 3 مجموعات OH ، - الجليسرين. الصيغة المشتركة للمركبات من هذا النوع هي CnH2n-1 (OH) 3. من أجل فهم أفضل لخصائص وتطبيق الغليسيرين ومثالياته ، دعونا ننظر في أنواع صيغ الصيغ ، كل منها يستخدم في حالات معينة.
تصنيف وتسميات الجلسرين
في الكيمياء العضوية ، والكحول هي المواد ،مشتقات الهيدروكربونات. يتم استبدال بعض ذرات الهيدروجين في الجزيئات بواحدة أو أكثر من مجموعات الهيدروكسيل. تختلف الكحولات في عدد مجموعات OH (أحادية ، مزدوجة - polyatomic). أقل ممثلي الطبقة مع عدد ذرات الكربون من 1 إلى 12 هي مواد سائلة ، وأعلى منها هي مواد صلبة. Alcantriols ، أو الجلسرين ، هي كحوليات triatomic التي تحتوي على ثلاثة hydroxyls ملزمة لثلاث ذرات الكربون المختلفة. تظهر المركبات التي تنتمي إلى هذه المجموعة خصائص amphoteric بسبب التأثير المتبادل لمجموعة hydroxy والراديكالية.
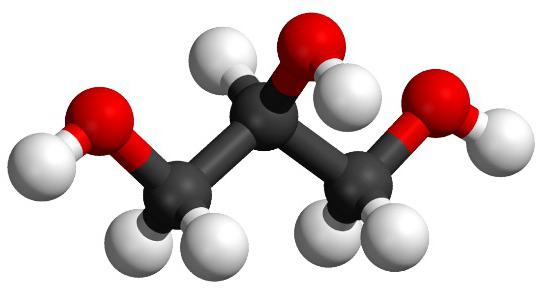
أبسط ممثل من alkantriols هو propanetriol - 1،2،3 (مرادف هو الجليسرين). صيغة الجوهر - ج3H8O3. يفترض التسميات المنهجيةذكر اسم alkane المقابل مع كلمة "triol" ، واستخدام الأرقام العربية التي تحدد موقف مجموعة OH. الترقيم في جزيئات homologs من الجليسرين هو من أقرب إلى نهاية سلسلة الهيدروكسيل. أنواع ممكنة من isomerism: هيكل سلسلة الكربون ، وموضع مجموعات الهيدروكسي ، البصرية.
اكتشاف الجلسرين

تلقى الصيدلاني السويدي ك. شيله في عام 1779 عندما تصبن الدهون لأول مرة مادة حبة جديدة. في 33 عاما دعا الفرنسي م. شفلر الجليسرين السائل الحلو.
تم تأسيس التركيب الكيميائي بواسطة Peluz في عام 1836. تم تقديم مساهمة كبيرة في دراسة الهيكل من قبل Berthelot (1854) و Wurz (1857) ، الذي استمر في التحقيق في الجلسرين. سمحت لنا الصيغة الجزيئية وطبيعة الراديكالي بتصنيف الجلسرين كالكحول المحدد.
زادت الحاجة إلى الغليسرين بشكل ملحوظبعد عام 1847 ، عندما تم اكتشاف إستر حامض النيتريك. تمكن المهندس السويدي أ. نوبل في عام 1875 من الحصول على مساعدة من المتفجرات الغليسيرين - الديناميت.
تكوين وبنية وأبسط صيغة من الجليسرين
يتطابق أبسط سجل لتكوين المادة مع الصيغة الحقيقية والتجريبية والجرأة للجليسيرين-سي3H8O3. تتكون السلسلة الكربونية من 3 ذرات ، كل منهاهم ملزمون بمجموعة الهيدروكسي. تشير الرموز الكيميائية إلى الذرات المكونة للمادة: C - الكربون ، O - الأكسجين ، H - hydrogen. تركيبة الجليسرين تعكس الصيغ المختلفة (الجزيئية والبنيوية). وتستخدم على نطاق واسع نماذج Sharoenergetic ونصف كروي في دراسة المادة. الهياكل ثنائية الأبعاد وثلاثية الأبعاد التي تم إنشاؤها بواسطة محاكاة الكمبيوتر هي صور مكانية لجزيء من الجلسرين. إنها تسمح لنا بتصور التركيبة والترتيب المتبادل والمسافة ، وزاوية الرابطة بين الذرات.

الجزيئات الجزيئية والمولية من الجلسرين
بواسطة الصيغة فمن الممكن العثور على الجزيئية والأضحيةكتلة ، نسبة العناصر في المادة. بالنسبة للحسابات ، من الضروري استخدام الكتل الذرية للعناصر المشار إليها في الجدول الدوري. صيغة تجريبية من الجلسرين: C3H5(OH)3. بضرب الكتلة الذرية (في ae m.) من كل عنصر من عدد من الذرات ، تليها إضافة القيم التي تم الحصول عليها ، نجد جزيئات (السيد) والجزيئية (M). لهذا النوع من الحسابات يكون من الملائم استخدام الصيغة الإجمالية للجليسيرين-سي3H8O3.
- Ar (H) = 1.00794؛ عدد الذرات في الجزيء هو 8.
- Ar (C) = 12.0107؛ ذرات - 3.
- Ar (O) = 15.9994؛ ذرات - 3.
- السيد (من3H8يا3) = 12.0107 * 3 + 1.00794 * 8 + 15.9994 * 3 = 92.09382 a. ه م.
- م (ج3H8يا3) = 92.09382 غرام / مول /
- نسبة العناصر في جزيء المادة: H - 8،756٪، C - 39،125٪، O - 52،119٪.

صيغة عقلانية وهيكلية الغليسيرين
تكوين المادة وجزيئاتها تعكسصيغة عقلانية وإجمالية ، لكنها لا تعطي فكرة عن ترتيب الذرات ، والتي تتميز الجلسرين. هي صيغة هيكلية ونموذج الكمبيوتر أكثر ملاءمة لدراسة بنية الجزيء ، الروابط بين الذرات.
- صيغة عقلانية من الجليسرين - C3H5(OH)3 . من تكوين الجزيء ، يتم فصل مجموعات OH الوظيفية وإرفاقها بين قوسين. مباشرة خلف قوس الإغلاق هو عدد مجموعات الهيدروكسي في الجزيء.
- الشكل النصف موسع للصيغة العقلانية هو HOCH2CH (OH) CH2OH (الجلسرين).
- تُظهر الصيغة البنائية في الشكل البياني ترتيب الجزيء. إن الشرط بين الذرات يرمز إلى الروابط الكيميائية.
- يحتوي هيكل لويس على نقاط تدل على إلكترونات التكافؤ والأزواج المشاركين في تكوين السندات.
بعض أنواع الصور للجزيء تأخذ الكثير من المساحة ، لذلك ، غالباً ما تستخدم الصيغ المختصرة ، على سبيل المثال ،2-CHOH-CH2OH ، وكذلك الهياكل العظمية:
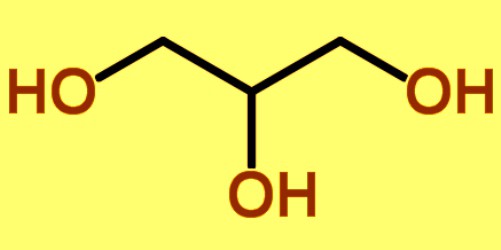
حالة الذرات في جزيء الجليسرين
الهيدروكسيل هو جسيم قطبي ، إلى جانب الأكسجينلديه زوج غير مشترك من الإلكترونات. يؤدي وجود ثلاث مجموعات هيدروكسي إلى مزيد من الاستقطاب لسندات O-H. ذرات الكربون يظهر تهمة جزئي "+" تسهيل استبدال محب للنواة من الهيدروكسيل. تم تأكيد خصائص التركيبة والهيكل ، والتي تعكس الصيغة البنائية للجليسيرين ، في خواص المادة. يتميز هذا المركب بالعديد من الجسور الهيدروجينية - روابط إضافية ضعيفة. يتميز الجليسرين بخصائص حمضية أكثر وضوحًا ، مقارنة بالإيثانول والبروبانول. من بين أهم المشتقات ثلاثي الجليسرول. الصيغة:
- أبسط هو C57H104يا6.
- نصف عقل مكشوف - (سي17H33COO)3C3H5.
- عقلانية مع عناصر الهيكلية والهيكل العظمي -

ظهور الجلسرين
في درجة حرارة الغرفة ، propanetriol-1،2،3-سائل عديم اللون أو أصفر شاحب ، عديم الرائحة ، حلوة إلى الذوق. يذوب الجليسرين ، الذي يصلب عند درجات حرارة منخفضة ، عند درجة حرارة 17.8 درجة مئوية. يبدأ غليان المادة متبوعًا بالتبخر عند 290 درجة مئوية. الجليسرين أثقل قليلاً من الماء ، وحساب كثافته عند 20 درجة مئوية يعطي قيمة 1.2604 جم / سم 3.

خصائص propanthriol - 1،2،3
الصيغة الكيميائية للغليسرين لا تعطيتمثيل الطبيعة amphoteric من الاتصال. الخصائص الحمضية والأساسية ضعيفة من المواد ذات الصلة لتأثير الميزات الذرات في الجزيء، والاستقطاب في مجموعة G-H. في ظل وجود الجلسرين يتفاعل مع هيدروكسيد القلوي والنحاس (II)، التي تم الحصول عليها اللون الأزرق مجمع (واحد من ردود الفعل النوعية). مع الأحماض ، يتم الانتهاء من رد فعل الجلسرين عن طريق تشكيل استرات. تفاعل كحول triatomic مع حمض النيتريك في وجود H2SO4 (conc.) يؤدي إلى تشكيل النتروجليسرين.
في المنزل من الدهون والزيوت بمساعدةيتم الحصول على الجليسرين ، الكحول الإيثيلي ، المكونات الأخرى ، والصابون. تتطلب عملية التحضير تسخينًا دقيقًا للكتلة في حمام مائي ، موقفا خلاقا لاختيار المكونات والأشكال لمنتج الصابون النهائي.
يستخدم الجليسرين ومشتقاته في المينا ،الدهانات ، العديد من الأدوية ، مستلزمات النظافة. توجد مادة حلوة في مجموعة متنوعة من الأطعمة ، بما في ذلك منتجات المخابز. الاسم الدولي للمحلويات والنكهات الحلويات - E422. جنبا إلى جنب مع غيرها من الكحول ، فضلا عن استرات الأحماض الدهنية ، يعتبر الجلسرين كبديل محتمل للوقود المشتق من النفط. ستؤدي الأساليب الاقتصادية لاستخدام أنواع جديدة من وقود الديزل الحيوي لتزويد السيارات بالوقود إلى إحداث ثورة في اقتصاد النقل العالمي. سوف يتحسن الوضع البيئي بشكل كبير ، وسيتراجع اعتماد الاقتصاد العالمي على إنتاج النفط والغاز.
</ p>